Como dijimos en otras entradas, los bioelementos se unen a través de enlaces químicos para formar biomoléculas más estables.
Las biomoléculas inorgánicas son aquellas que aparecen también fuera de la materia viva y que no es única de ella, como el agua, las sales minerales y los gases.
En esta entrada, en concreto, abordaremos el caso del agua:
EL AGUA
El agua es la molécula más abundante de los seres vivos, y representa entre el 70% y el 90% del peso de la mayor parte de los organismos.
La gran importancia del agua deriva de la inmensa mayoría de las reacciones bioquímicas que se desarrollan en su seno, lo que se debe a su estructura química.
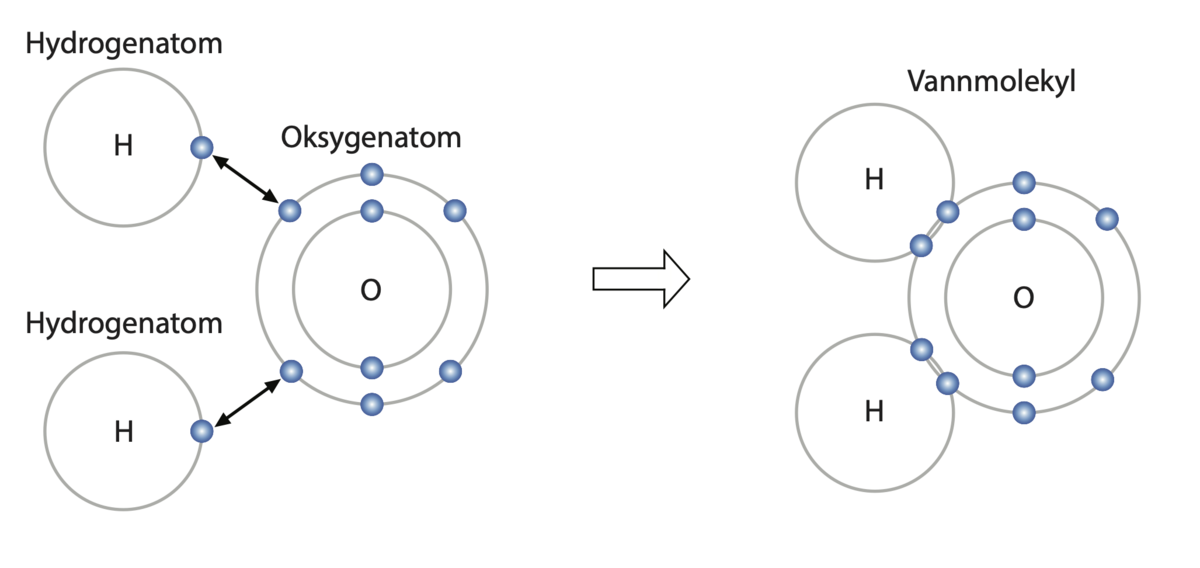
Molécula de agua: se puede observar cómo se comparten electrones a través del enlace covalente. Mientras que el átomo de oxígeno comparte 2 electrones, cada átomo de Hidrógeno aporta 1.
ESTRUCTURA QUÍMICA DEL AGUA
Como sabemos, la fórmula del agua es H₂O, es decir, cada molécula está constituida por un átomo de Oxígeno y dos átomos de Hidrógeno.
Estos dos elementos químicos están unidos por enlace covalente, unión en la que se comparten electrones, siendo en este caso concreto 2 por parte del Oxígeno y 1 por cada elemento de Hidrógeno.
Sin embargo, como todo en la vida, siempre que se comparte algo, hay personas más egoístas y otras más generosas.
Así, el oxígeno es más avaricioso, es decir, atrae hacia sí ese par de electrones compartidos. Este fenómeno se debe a que es más electronegativo, siendo el término correcto para definir a este fenómeno.

Enlaces de Hidrógeno en las moléculas de agua. Como se puede observar, cada molécula puede establecer dicho enlace con otras 4. Dicha interacción se produce por la atracción electrostática entre la carga parcial positiva del Hidrógeno de una molécula y la negativa del Oxígeno de la molécula adyacente.
Por su parte, el Hidrógeno es más generoso, en otras palabras, menos electronegativo y, por consiguiente, su “fuerza de atracción de los electrones hacia sí es prácticamente nula”.
En consecuencia, sabiendo que el electrón tiene carga negativa y que el oxígeno lo atrae con más fuerza, es evidente que este átomo tendrá una carga parcial negativa (-) y el Hidrógeno una carga parcial positiva (+).
Como resultado, tenemos una molécula polar, diferenciando un polo positivo (el Hidrógeno) y otro negativo (el Oxígeno).
De las razones antes mencionadas se puede inferir que, si se aproximan varias moléculas de agua lo suficiente, se establece una atracción electrostática entre la carga parcial negativa del átomo de O y la carga parcial positiva de un átomo de H de la molécula adyacente.
Dicha interacción es lo que conocemos como puente o Enlace de Hidrógeno, permitiendo que cada molécula de agua pueda interaccionar con hasta cuatro vecinas.
PROPIEDADES DEL AGUA
- EL HIELO FLOTA SOBRE AGUA LÍQUIDA: los enlaces de hidrógeno tienen un tiempo de vida muy corto, rompiéndose y formándose constantemente en el estado líquido, mientras que en estado sólido las moléculas se disponen formando un tetraedro estable. Esto implica que en estado sólido las moléculas están más alejadas entre sí que en estado líquido, lo que explica que el hielo sea menos denso que el agua. Este simple hecho permite la vida acuática submarina y que exista tanta cantidad de agua líquida en nuestro planeta.
- ELEVADA FUERZA DE ADHESIÓN Y COHESIÓN ENTRE SUS MOLÉCULAS: lo que permite su elevada tensión superficial (la superficie del agua se comporta como una membrana elástica tensa), su incompresibilidad (no puede comprimirse y actúa como esqueleto hidrostático) y la capilaridad (permite el ascenso del agua a lo largo de tubos largos y estrechos, como el transporte de savia en las plantas).
- ELEVADO CALOR ESPECÍFICO Y DE VAPORIZACIÓN: para aumentar la temperatura del agua se necesita muchísima energía, por lo que es utilizado como termorregulador por la mayoría de los seres vivos, como, por ejemplo, la sudoración.
- ELEVADA CONSTANTE DIELÉCTRICA: permite mantener separados iones de carga opuesta, lo que conlleva una fácil disolución de las sales y otros compuestos iónicos.
- GRAN CAPACIDAD DE DISOLUCIÓN: debido a que puede formar enlaces de Hidrógeno con otras moléculas polares como aminoácidos, monosacáridos…
- CAPACIDAD DE DISOCIACIÓN EN H+ Y OH-: lo que le permite participar en infinidad de reacciones químicas, como las ácido-base o de hidrólisis.
Aquí os dejo un pequeño fragmento de un vídeo mío correspondiente a esta temática que, espero, aclare estas propiedades:
COMPORTAMIENTO DE LAS MOLÉCULAS EN FUNCIÓN DE SU RELACIÓN CON EL AGUA
- Sustancia hidrofílica: fácilmente soluble en agua, por ser moléculas polares que permiten la interacción con la molécula de H₂O a través de enlaces de Hidrógeno.
- Sustancia hidrofóbica: difícilmente soluble en agua por ser moléculas apolares, no permitiendo la interacción con la molécula de H₂O a través de enlaces de Hidrógeno.
- Sustancias anfipáticas: aquellas que tienen una región hidrofílica y otra hidrofóbica, permitiendo, por un lado, una interacción con la molécula de agua y, por otro, una interacción solo con moléculas hidrofóbicas. Es el típico caso de los fosfolípidos, formando instantáneamente micelas y bicapas lipídicas, estas últimas las integrantes de la membrana celular.